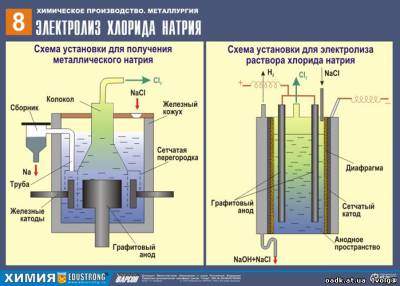
Совокупность ОВР ,
которые протекают на электродах в растворах или расплавах электролитов при пропускании через них электрического тока, называют электролизом.На катоде источника тока происходит процесс передачи электронов катионам из раствора или расплава, поэтому катод является «восстановителем». На аноде происходит отдача электронов анионами, поэтому анод является «окислителем».
При электролизе как на аноде, так и на катоде могут происходить конкурирующие процессы.
При проведении электролиза с использованием инертного (нерасходуемого) анода (например, графита или платины), как правило, конкурирующими являются два окислительных и восстановительных процесса:
на аноде — окисление анионов и гидроксид-ионов, на катоде — восстановление катионов и ионов водорода.
При проведении электролиза с использованием активного (расходуемого) анода процесс усложняется и конкурирующими
реакциями на электродах являются следующие:
на аноде — окисление анионов и гидроксид-ионов, анодное растворение металла — материала анода;
на катоде — восстановление катиона соли и ионов водорода, восстановление катионов металла, полученных при растворении
анода.
При выборе наиболее вероятного процесса на аноде и катоде исходят из положения, что протекает та реакция, которая требует наименьшей затраты энергии. При электролизе растворов солей с инертным электродом используют следующие правила.
1. На аноде могут образовываться следующие продукты:
а) при электролизе растворов, содержащих анионы F-, SО42- , NO3-, РO43-, ОН- выделяется кислород;
б) при окислении галогенид-ионов выделяются свободные галогены ;
в) при окислении анионов органических кислот происходит процесс:
2RCOO- - 2е → R-R + 2СО2.
2. При электролизе растворов солей , содержащих ионы , расположенные в ряду напряжений левее Аl3+, на катоде выделяется водород; если ион расположен правее водорода, то выделяется металл.
3. При электролизе растворов солей, содержащих ионы, расположенные между Аl3+ и Н+ на катоде могут протекать конкурирующие процессы как восстановления катионов, так и выделения водорода.
Рассмотрим в качестве примера электролиз водного раствора хлорида меди на инертных электродах. В растворе находятся ионы Cu2+ и Cl-, которые под действием электрического тока направляются к соответствующим электродам:
<>
| CuCl2 |
|
| ↓ |
|
|
| (-) Катод ← Cu2+ | + | 2Cl- → Анод (+) |
| Cu2+ + 2e = Cu0 |
| 2Cl- - 2e = Cl2 |
На катоде выделяется металлическая медь , на аноде — газообразный хлор.
Если в рассмотренном примере электролиза раствора СuCl2 в качестве анода взять медную пластинку, то на катоде выделяется медь, а на аноде, где происходят процессы окисления, вместо разрядки ионов Сl и выделения хлора протекает окисление анода (меди). В этом случае происходит растворение самого анода, и в виде ионов Сu2+ он переходит в раствор. Электролиз СuCl2 с растворимым анодом можно записать так:
| CuCl2 |
|
| ↓ |
|
| (-) Катод ← Cu2+ | + | 2Cl- → Анод (+) |
| Cu2+ + 2e = Cu0 |
| 2Cu- - 2e = Cu2+ |
Таким образом, электролиз растворов солей с растворимым анодом сводится к окислению материала анода (его растворению) и сопровождается переносом металла с анода на катод. Это свойство широко используется при рафинировании (очистке) металлов от загрязнений.
Для получения высокоактивных металлов (калия, алюминия и др.), легко вступающих во взаимодействие с водой, применяют электролиз расплава солей или оксидов, например
<>
| Al2O3 |
|
| ↓ | расплав |
| (-) катод ← 2Al3+ | + | 2Cl- → анод (+) (С – графит) |
| 2Al3+ + 6e = 2Al0 |
| 3O2- - 6e = 3/2O2 |
|
| 2C + O2 = 2CO |
|
| 2CO + O2 = 2CO2 |
При электролизе водного раствора соли активного металла кислородсодержащей кислоты (например, КNО3) ни катионы металла, ни ионы кислотного остатка не разряжаются. На катоде выделяется водород, а на аноде — кислород, и электролиз раствора нитрата калия сводится к электролитическому разложению воды.
Отметим, что электролиз растворов электролитов проводить энергетически выгоднее, чем расплавов, так как электролиты плавятся при очень высоких температурах.
Зависимость количества вещества, образовавшегося при электролизе, от времени и силы тока описывается обобщенным законом Фарадея:
m = (Э / F) • I • t = (М / (n • F)) • I • t,
где m — масса образовавшегося при электролизе вещества (г); Э — эквивалентная масса вещества (г/моль); М — молярная масса вещества (г/моль); n — количество отдаваемых или принимаем электронов; I — сила тока (А); t — продолжительность процесса (с); F — константа Фарадея, характеризующая количество электричества, необходимое для выделения 1 эквивалентной массы вещества (F= 96500 Кл/ моль = 26,8 А• ч / моль).
.
Расплавы
1) Активные металлы
1.Соль активного металла и бескислородной кислоты
NaCl ↔ Na+ + Cl−
K"катод"(-): Na+ + 1e = Na0
A"анод"(+): Cl− — 1e = Cl0; Cl0+Cl0=Cl2
Вывод: 2NaCl → (электролиз) 2Na + Cl2
2.Соль активного металла и кислородосодержащей кислоты
Na2SO4↔2Na++SO42−
K(-): 2Na+ +2e =2Na0
A(+): 2SO42− −4e =2SO3+O2
Вывод: 2Na2SO4 → (электролиз) 4Na + 2SO3 + O2
3. Гидроксид: активный металл и гидроксид-ион
NaOH ↔ Na+ + OH−
K(-): Na+ +1e =Na0
A(+): 4OH− −4e =2H2O + O2
Вывод: 4NaOH → (электролиз) 4Na + 2H2O + O2
2) Менее активные металлы
Точно так же
3) Неактивные металлы
Точно так же
1) Активные металлы
1.Соль активного металла и бескислородной кислоты
NaCl ↔ Na+ + Cl−
K"катод"(-): 2H2O + 2e = H2 + 2OH−
A"анод"(+): Cl− — 1e = Cl0; Cl0+Cl0=Cl2
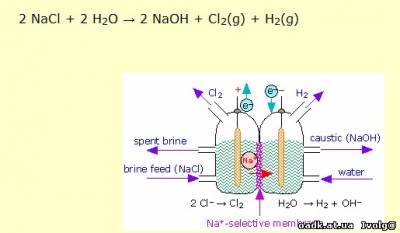
Вывод: 2NaCl + 2H2O(электролиз) → 2H2 + Cl2 +2NaOH
2.Соль активного металла и кислородсодержащей кислоты
Na2SO4↔2Na++SO42−
K(-): 2H2O + 2e = H2 + OH−
A(+): 2H2O — 4e = O2 + 4H+
Вывод: 2H2O (электролиз) → H2 + O2
3. Гидроксид: активный металл и гидроксид-ион
NaOH ↔ Na+ + OH−
K(-): 2H2O + 2e = H2 + 2OH−
A(+): 2H2O — 4e = O2 + 4Н+
Вывод: 2H2O (электролиз) → 2H2 + O2
2) Менее активные металлы
1.Соль менее активного металла и бескислородной кислоты
ZnCl2 ↔ Zn2+ + 2Cl−
K"катод"(-): Zn2+ + 2e = Zn0
A"анод"(+): 2Cl− — 2e = 2Cl0
Вывод: ZnCl2 (электролиз) → Zn + Cl2
2.Соль менее активного металла и кислородсодержащей кислоты
ZnSO4 ↔ Zn2++SO42−
K(-): Zn2+ + 2e = Zn0
A(+): 2H2O — 4e = O2 + 4Н+
Вывод: 2ZnSO4 + 2H2O(электролиз) → 2Zn + 2H2SO4 + O2
3. Гидроксид: невозможно (нерастворим)
3) Неактивные металлы
Точно так же
.